纳武单抗 的亲和力非常强,可以在非常低的浓度下(~1.5 ng/mL)解除PD-L1对T细胞的抑制,增强T细胞的活性。与此同时,在没有抗原或者T细胞受体存在的情况下,它也不影响T细胞的活性。科研人员发现在0.003到50μg/mL浓度区间内,nivolumab对T细胞没有出 ...

伊匹单抗 的成功,让Medarex的科研人员更加意识到,CTLA-4及其类似靶点的单抗药物必将是肿瘤药开发的方向。在Medarex转基因小鼠技术带头人Nils Lonberg的带领下,科研人员开始检索新线索,他们竟然意外地发现日本京都大学本庶佑教授(2018诺贝尔医学/生 ...
癌症,说到底就是人体免疫系统与异常细胞之间的一场战斗。癌症会不会发生,看的就是在这场战斗里谁强谁弱。百年以来,科学家一直在探索激活人体免疫系统以治疗癌症的 免疫疗法 ,希望的曙光初现于1996年。 是年加州大学伯克利分校的James Allison团 ...
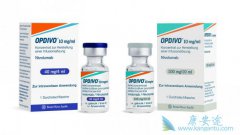
纳武单抗 (nivolumab),这个在中国叫“欧狄沃”(商标:Opdivo)的PD-1免疫抑制剂终于在国内通过正规渠道可以买到,欧狄沃在全球已获批用于9个瘤种,17项适应症,是至今全球适应症最多的PD-1抑制剂。 欧狄沃是在全球范围内首款获批的抗PD-1抗体,可 ...
非小细胞肺癌 分为鳞状细胞癌和非鳞状非小细胞肺癌,我们再来一起看看针对鳞状非小细胞肺癌的KEYNOTE-407研究。2018年9月25日,KEYNOTE-407的最新研究在WCLC会议(世界肺癌大会)上发布,研究发现“K药”联合卡铂和紫杉类化疗相比于单纯化疗,可以显著 ...
10月16日,PD-1的K药(也就是 Keytruda ,帕博利珠单抗,下面简称K药),向中国CFDA提交基于KEYNOTE-407研究数据的治疗申请,将K药联合化疗用于转移性鳞状非小细胞肺癌的一线治疗。所谓的一线治疗,也就是病人在确诊病情之后第一次治疗使用的治疗药物。K ...
2018年初, 乳腺癌患者 迎来了重磅喜讯:奥拉帕尼正式获批用于治疗具有或疑似具有种系BRCA突变、人类表皮生长因子受体2(HER2)阴性、并曾接受过化疗的转移性乳腺癌患者。第一种批准用于治疗种系BRCA突变转移性乳腺癌患者的PARP抑制剂。 这项批准是 ...
作为全球首个获批的多聚二磷酸腺苷核糖聚合酶[poly(ADP-ribose)polymerase](PARP)抑制剂,2013年 奥拉帕尼 首次用于治疗卵巢癌患者,最早于2014年12月以胶囊剂型获批用于治疗既往接受过三线以上化疗的BRCA突变晚期卵巢癌。接下来,小编带大家回顾一下 ...
2018年10月16日,美国食品和药物管理局(FDA)批准了辉瑞公司的靶向抗癌药talazoparib( TALZENNA ),talazoparib是一种PARP抑制剂,用以治疗携带有害或怀疑有害的生殖系BRCA突变,HER2阴性的局部晚期或转移性乳腺癌患者。FDA还批准了BRACAnalysis CDx检测( ...
对于大部分人来说,罹患癌症已是极为不幸,而癌症发生 脑转移 ,则基本等同于被判“死刑”。癌症的脑转移是指原发于身体其他部位的肿瘤细胞转入颅内,是治疗难度极高的一种情况。数据显示,20%-40%的癌症患者会出现脑转移,其中以肺癌脑转移最为常见,其 ...

PARP抑制剂目前是乳腺癌治疗的创新型药物。新一代的PARP抑制剂 Talzenna 的获批,是基于III期临床研究EMBRACA(NCT01945775)的数据。该研究在431例gBRCAm、HER2阴性局部晚期或转移性乳腺癌患者中开展,评估了talazoparib相对于医生选择的标准单药化疗方 ...
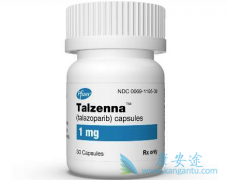
辉瑞(Pfizer)制药宣布:美国食品和药物管理局(FDA)已批准靶向抗癌药 Talzenna (talazoparib),用于存在有害或疑似有害的生殖系BRCA突变(gBRCAm)、HER2阴性局部晚期或转移性乳腺癌(MBC)患者的治疗。 talazoparib是一种聚ADP-核糖聚合酶(PA ...

目前, PARP抑制剂 市场由阿斯利康研发的奥拉帕利主导。自2014年年底该药物在欧美获批上市以来,一路畅销。阿斯利康财报显示,15-17年奥拉帕利销售额分别为0.94亿美元、2.18亿美元、2.97亿美元。2017 年全球PARP 抑制剂的销售额为4.62 亿美元,其中,奥 ...

日前,辉瑞公司 Talzenna 在美获批,用于治疗遗传性基因突变相关的HER2阴性局部晚期或转移性乳腺癌。所谓遗传性基因突变,即BRCA突变。自此,Talzenna成为在美获批的第四款PARP抑制剂。 PARP和BRCA这两个基因之间,渊源颇深,它们均负责修复细胞内DN ...
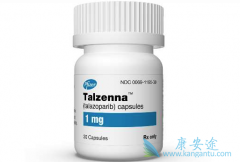
与标准化疗组相比, Talazoparib 治疗组的客观反应率提高一倍(62.6% vs 27.2%,p<0.001)。Talazoparib组和标准化疗组的反应持续时间(DOR)分别为5.4个月vs. 3.1个月。虽然总生存数据尚不成熟,但中期分析时,与标准化疗组相比,Talazoparib组的中位O ...
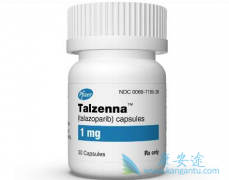
2018年10月16日, Talzenna (Talazoparib)获得美国FDA批准上市,用于治疗携带胚系BRCA突变(有害或疑似有害),HER2阴性的局部晚期或转移性乳腺癌患者。Talazoparib是辉瑞公司研发的新一代PARP抑制剂,临床前研究显示,Talazoparib有较强的催化阻滞活 ...
胃肠道间质瘤 (Gastrointestional Stromal Tumor,GIST)是胃肠道最常见的间叶源性肿瘤,约占消化道肿瘤的1~3%。GIST在生物学行为上可从良性发展至恶性,免疫组化检测通常表达CD117和DOG1阳性,大多数病例具有c-KIT或血小板源性生长因子受体α多肽(p ...

整个全球对于 ALK抑制剂 研发的进步是非常神速的,有一代克唑替尼,二代色瑞替尼、艾乐替尼、Brigatinib,已经获得了美国FDA审批适应证,还有三代劳拉替尼也正在进行三期随机对照临床研究,结果也将很快向公众公布。阿来替尼也已经在中国上市。所以对中 ...
2018年AACR上,研究者报道:对21807名晚期肿瘤患者(包括50余种肿瘤)的血液样本进行了深度测序,检测和分析了70多个和癌症相关的基因变异情况。结果发现,在85%(18503/21807)的所有肿瘤类型中检测到体细胞ctDNA突变。同时,该研究还分析了不同癌种之间 ...
“药王”的称号也带来了众多 Humira 的模仿者,也就是生物类似药。2016年9月23日,FDA宣布批准Amgen的Amjevita上市,这是FDA批准的首个Humira的生物类似药;2017年3月22日,Amgen宣布EMA批准其Amgevita,这是首个在欧盟获批的Humira的生物类似药。截止到 ...
免费咨询电话:4000 980 586
微信咨询

扫描二维码
免费咨询医学博士